Μοριακός και δομικός τύπος φαινόλης
Οι φαινόλες είναι η κοινή ονομασία για τις αρωματικές αλκοόλες. Με τις ιδιότητές τους, οι ουσίες είναι ασθενή οξέα. Μεγάλη πρακτική σημασία έχουν πολλά ομόλογα υδροξυβενζολίου C6H50H (τύπος φαινόλης) - ο απλούστερος εκπρόσωπος της κατηγορίας. Ας εξετάσουμε αυτό το θέμα με περισσότερες λεπτομέρειες.
Φαινόλες. Γενικός τύπος και ταξινόμηση
Ο γενικός τύπος των οργανικών ουσιών που σχετίζονται μεαρωματικές αλκοόλες, - R-OH. Τα μόρια των φαινολών και των κρεζολών που σχηματίζονται κανονικά σχηματίζονται από τη ρίζα - φαινύλ C6H5, με την οποία συνδέονται άμεσα μία ή περισσότερες υδροξυλομάδες ΟΗ (υδροξυομάδες). Με τον αριθμό τους σε ένα μόριο, οι φαινόλες ταξινομούνται σε μονές, διπλές και πολυατομικές. Μονατομικές ενώσεις αυτού του τύπου είναι φαινόλη και κρεσόλη. Τα πιο κοινά μεταξύ των πολυυδρικών υδροξυβενζολών είναι οι ναφθόλες, οι οποίες περιέχουν 2 συμπυκνωμένους πυρήνες στη σύνθεσή τους.

Η φαινόλη αντιπροσωπεύει αρωματικές αλκοόλες
Η φαινόλη ήταν ήδη γνωστή στους υφαντουργούς ήδη από τον 18ο αιώνα: οι υφαντές το χρησιμοποιούσαν ως βαφή. Στην απόσταξη λιθανθρακόπισσας το 1834, ο γερμανός χημικός F. Runge διακρίνει κρυστάλλους αυτής της ουσίας με χαρακτηριστική γλυκιά μυρωδιά. Η λατινική ονομασία του άνθρακα είναι carbo, έτσι η ένωση ονομάστηκε καρβολικό οξύ (καρβολικό οξύ). Ο γερμανός ερευνητής δεν κατάφερε να προσδιορίσει τη σύνθεση της ουσίας. Ο μοριακός τύπος της φαινόλης δημιουργήθηκε το 1842 από τον O. Laurent, ο οποίος θεωρούσε το καρβολικό παράγωγο του βενζολίου. Για το νέο οξύ που χρησιμοποιείται το όνομα "φαινύλιο". Ο Charles Gerard διαπίστωσε ότι η ουσία είναι αλκοόλη και την ονόμασε φαινόλη. Οι αρχικές περιοχές εφαρμογής της ένωσης είναι φάρμακα, μαυρίσματος δέρματος, παραγωγή συνθετικών βαφών. Χαρακτηριστικά της ουσίας:
- Ορθολογικός χημικός τύπος - C6H5OH.
- Το μοριακό βάρος της ένωσης είναι 94.11 α. ε. m.
- Ο ακαθάριστος τύπος, ο οποίος αντικατοπτρίζει τη σύνθεση, είναι ο C6H6Ο.

Ηλεκτρονική και χωρική δομή του μορίου φαινόλης
Ο κυκλικός δομικός τύπος του βενζολίου πρότεινεΟ γερμανικός οργανικός χημικός F. Kekule το 1865, και λίγο πριν από αυτόν - ο I. Loschmidt. Οι επιστήμονες αντιπροσώπευαν ένα μόριο οργανικής ύλης με τη μορφή ενός κανονικού εξαγώνου με εναλλασσόμενους απλούς και διπλούς δεσμούς. Σύμφωνα με τις σύγχρονες ιδέες, ο αρωματικός πυρήνας είναι ένα ειδικό είδος δακτυλιοειδούς δομής, που ονομάζεται "συζευγμένη σύνδεση".
Έξι άτομα άνθρακα C υποβάλλονται στη διαδικασία sp2- υβριδισμός ηλεκτρονικών τροχιακών. Τα σύννεφα ρ-ηλεκτρονίων, τα οποία δεν συμμετέχουν στο σχηματισμό δεσμών C-C, αλληλεπικαλύπτονται πάνω και κάτω από το επίπεδο του πυρήνα του μορίου. Υπάρχουν δύο μέρη του γενικού ηλεκτρονικού σύννεφου, το οποίο καλύπτει ολόκληρο το δαχτυλίδι. Ο δομικός τύπος της φαινόλης μπορεί να φαίνεται διαφορετικός, δεδομένης της ιστορικής προσέγγισης της περιγραφής της δομής του βενζολίου. Για να τονιστεί η ακόρεστη φύση των αρωματικών υδρογονανθράκων, τρεις από τους έξι δεσμούς συμβατικά θεωρούνται διπλοί, οι οποίοι διασκορπίζονται με τρεις απλούς.
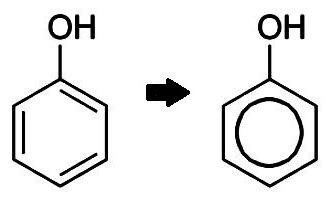
Πόλωση του δεσμού στην υδροξυομάδα
Στον απλούστερο αρωματικό υδρογονάνθρακα - βενζόλιο C6H6 - το νέφος ηλεκτρονίων είναι συμμετρικό. Ο τύπος φαινόλης διαφέρει από μία ομάδα υδροξυλίου. Η παρουσία υδροξυλίου διαταράσσει τη συμμετρία, η οποία αντικατοπτρίζεται στις ιδιότητες της ουσίας. Ο δεσμός μεταξύ οξυγόνου και υδρογόνου στην ομάδα υδροξυλίου είναι πολικός ομοιοπολικός. Η μετατόπιση του γενικού ζεύγους ηλεκτρονίων στο άτομο οξυγόνου οδηγεί στην εμφάνιση ενός αρνητικού φορτίου (μερικό φορτίο) επάνω του. Το υδρογόνο στερείται ηλεκτρόνιου και αποκτά μερική φόρτιση του "+". Επιπλέον, το οξυγόνο στην ομάδα Ο-Η είναι ο ιδιοκτήτης δύο ζευγών ηλεκτρονίων που δεν μοιράζονται. Ένας από αυτούς προσελκύεται από ένα ηλεκτρονικό σύννεφο ενός αρωματικού πυρήνα. Για το λόγο αυτό, ο δεσμός γίνεται πιο πολωμένος, το άτομο υδρογόνου αντικαθίσταται ευκολότερα από μέταλλα. Τα μοντέλα δίνουν μια ιδέα για τον ασύμμετρο χαρακτήρα του μορίου της φαινόλης.
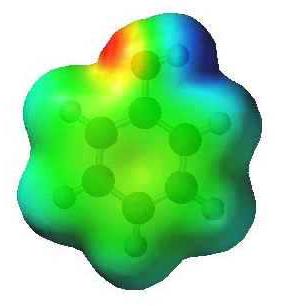
Ιδιαιτερότητες της αλληλεπίδρασης των ατόμων σε φαινόλη
Ένα ενιαίο ηλεκτρονικό σύννεφο του αρωματικού πυρήνα στοτο μόριο φαινόλης αντιδρά με την ομάδα υδροξυλίου. Υπάρχει ένα φαινόμενο που ονομάζεται σύζευξη, ως αποτέλεσμα του οποίου το φυσικό ζεύγος ηλεκτρονίων του ατόμου οξυγόνου της ομάδας υδροξυλίου προσελκύεται από το σύστημα κύκλου βενζολίου. Η μείωση στο αρνητικό φορτίο αντισταθμίζεται από μια ακόμη μεγαλύτερη πόλωση του δεσμού στην ομάδα Ο-Η.
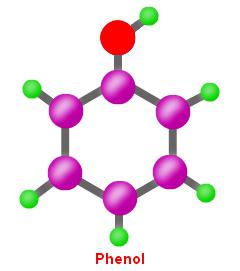
Ο αρωματικός πυρήνας αλλάζει επίσης το σύστημαηλεκτρονική διανομή. Μειώνει τον άνθρακα, ο οποίος σχετίζεται με το οξυγόνο και αυξάνεται κοντά στα πλησιέστερα άτομα στις ορθο-θέσεις (2 και 6). Η σύζευξη προκαλεί τη συσσώρευση μιας φόρτισης "-" πάνω τους. Περαιτέρω «πυκνότητα μετατόπισης - κίνησή του από τα άτομα στις μετα-θέσεις (3 και 5) προς άνθρακα στην παρα-θέση (4). Ο τύπος φαινόλης για την ευκολία μελέτης της σύζευξης και της αμοιβαίας επίδρασης συνήθως περιέχει την αρίθμηση των ατόμων του δακτυλίου βενζολίου.

Επεξήγηση των χημικών ιδιοτήτων της φαινόλης με βάση την ηλεκτρονική της δομή
Οι διεργασίες σύζευξης του αρωματικού πυρήνα καιυδροξύλιο επηρεάζουν τις ιδιότητες και των δύο σωματιδίων και ολόκληρης της ουσίας. Για παράδειγμα, μια υψηλή πυκνότητα ηλεκτρονίων στο άτομο στην ορθο και παρα θέσεις (2, 4, 6) καθιστά το C-H δεσμό ενός αρωματικού κύκλου φαινόλης πιο αντιδραστικό. Το αρνητικό φορτίο των ατόμων άνθρακα στις μετα-θέσεις μειώνεται (3 και 5). Επίθεση των ηλεκτρόφιλης σωματιδίων σε χημικές αντιδράσεις που εκτίθενται άνθρακα στην ορθο και παρα θέσεις. Στην αντίδραση βρωμίωσης του βενζολίου, οι αλλαγές συμβαίνουν με ισχυρή θέρμανση και παρουσία καταλύτη. Παρασκευάζεται μονοαλογόνο παράγωγο - βρωμοβενζόλιο. Ο τύπος φαινόλης επιτρέπει στην ουσία να αντιδρά με βρώμιο σχεδόν ακαριαία χωρίς θέρμανση του μίγματος.
Ο αρωματικός πυρήνας επηρεάζει την πολικότητα του δεσμού στουδροξύ, αυξάνοντας την. Το άτομο υδρογόνου γίνεται πιο κινητό, σε σύγκριση με τις περιοριστικές αλκοόλες. Η φαινόλη αντιδρά με αλκάλια, σχηματίζοντας φαινολικά άλατα. Αιθανόλη δεν αντιδρά με αλκάλια, ή μάλλον, τα προϊόντα της αντίδρασης - αιθανολικά - αποσυντίθενται. Χημικά, οι φαινόλες είναι ισχυρότερα οξέα από τις αλκοόλες.
Εκπρόσωποι της κατηγορίας αρωματικών αλκοολών
Ο γενικός τύπος του ομόλογου της φαινόλης-κρεζόλης (μεθυλφαινόλη, υδροξυτολουόλιο) -C7H8Η ουσία στις φυσικές πρώτες ύλες συχνά συνοδεύει φαινόλη, έχει επίσης αντισηπτικές ιδιότητες. Άλλα ομόλογα φαινόλης:
- Πυροκατεχίνη (1,2-υδροξυβενζόλιο). Χημικός τύπος - C6H4(ΟΗ)2.
- Ρεσορκινόλη (1,3-υδροξυβενζόλιο) -Ο6H4(ΟΗ)2.
- Pyrogallol (1,2,3-τριϋδροξυβενζόλιο) -C6H3(ΟΗ)3.
- Ναφθόλη. Ο ακαθάριστος τύπος της ουσίας είναι C10H7OH. Χρησιμοποιείται στην παραγωγή βαφών, φαρμάκων, αρωματικών ενώσεων.
- Τιμόλη (2-ισοπροπυλο-5-μεθυλοφαινόλη). Χημικός τύπος - C6H3CH3(ΟΗ) (C3H7). Χρησιμοποιείται στη χημεία της οργανικής σύνθεσης, της ιατρικής.
- Η βανιλλίνη, επιπλέον της φαινολικής ρίζας, περιέχει μία ομάδα αιθερικού εστέρα και ένα υπόλειμμα αλδεϋδης. Η ακαθάριστη φόρμουλα για την ένωση είναι C8H8Ο3. Η βανιλίνη χρησιμοποιείται ευρέως ως τεχνητό άρωμα.
Τύπος του αντιδραστηρίου για την αναγνώριση των φαινολών
Ο ποιοτικός προσδιορισμός της φαινόλης μπορεί να πραγματοποιηθεί μεχρησιμοποιώντας βρώμιο. Ως αποτέλεσμα της αντίδρασης υποκατάστασης, καθιζάνει ένα λευκό ίζημα τριβρωμοφαινόλης. Η πυροκατεχίνη (1,2-υδροξυβενζόλιο) έχει χρώμα πράσινη παρουσία διαλελυμένου χλωριούχου σιδήρου. Με το ίδιο αντιδραστήριο, η φαινόλη αντιδρά χημικά και σχηματίζεται τριφαινολικό, το οποίο έχει μωβ χρώμα. Μια ποιοτική αντίδραση στην ρεσορσινόλη είναι η εμφάνιση χρώσης σκούρου ιώδους παρουσία χλωριούχου σιδήρου. Σταδιακά το χρώμα της λύσης γίνεται μαύρο. Ο τύπος αντιδραστηρίου, ο οποίος χρησιμεύει στην αναγνώριση της φαινόλης και ορισμένων από τα ομόλογά της, είναι το FeCl3 (χλωριούχο σίδηρο).
Το υδροξυβενζόλιο, η ναφθόλη, η θυμόλη είναι όλες οι φαινόλες. Ο γενικός τύπος και η σύνθεση των ουσιών καθιστά δυνατό να προσδιοριστεί αν αυτές οι ενώσεις ανήκουν στην αρωματική σειρά. Όλες οι οργανικές ουσίες που περιέχουν στον τύπο τους ρίζα φαινυλίου C6H5, με τις οποίες οι υδροξυ ομάδες συνδέονται απ 'ευθείας,παρουσιάζουν ειδικές ιδιότητες. Διαφέρουν από τις αλκοόλες σε καλύτερη εκφρασμένη οξύτητα. Σε σύγκριση με τις ουσίες της ομόλογης σειράς βενζολίου, οι φαινόλες είναι πιο δραστικές χημικές ενώσεις.
</ p>



